- HOME
- 医療機器/体外診断用医薬品 製造販売業/選任製造販売業 薬事申請代行事業
医療機器/体外診断用医薬品
製造販売業/選任製造販売業
薬事申請代行事業
日本市場へ進出予定の
医療機器メーカー、体外診断用医薬品メーカの皆様へ
株式会社ICSTは国内外問わず医療機器、体外診断用医薬品市場への進出をサポートします。
MAH、DMAHサービス
について
医療機器/体外診断用医薬品の製造販売業取得は、人的要件、QMS省令、GVP省令への適合など多くの要件を満たす必要があります。 弊社では、日本に支社をもたない海外メーカー様、医療機器業界に参入を検討されているメーカー様等に代わり、国内外問わず(選任)製造販売業者として医療機器/体外診断用医薬品の薬事申請から市販後安全管理のサポートまでさせていただいております。
弊社では、お客様のご希望に沿いMAH、DMAHどちらの方式でもご対応させていただいております。
製造販売業とは
Marketing Authorization Holder
製造販売業者(MAH: Marketing Authorization Holder)とは、医薬品、医療機器、体外診断用医薬品などの製造(又は輸入)、品質管理、流通、販売後の安全管理を一貫に監督する事業者です。製造から市場供給までの全過程で法規制を遵守し、製品の品質・安全性確保と、市販後の安全管理(QMS・GVP省令)を保証する最終責任者となる業種です。自社製造だけでなく、他社に製造を委託(OEM/ODM)したり、海外製品を輸入したりする場合でも、その市場に出る製品全般に対する責任を負い、製造業(製造行為自体)とは区別されます。
製品の認証/承認取得した場合、MAHが認証/承認取得者となります。
日本国内で医療機器、体外診断用医薬品などを流通させるためにはMAHが不可欠になります。
選任製造販売業とは
Designated Marketing Authorization Holder
選任製造販売業者(DMAH: Designated Marketing Authorization Holder)とは、日本に事業所(または製造販売業者)を持たない外国の医療機器・体外診断用医薬品メーカーが日本で製品を販売する際に、日本国内で選任する製造販売業者のことです。
DMAH は、外国メーカーの承認取得と国内流通をサポートし、薬事申請業務、製品の品質管理、流通、市販後の安全管理までを一貫して監督する 法的責任者 となります。
具体的には、製造販売後安全管理基準(GVP)および品質管理基準(QMS)に基づき、製品の品質確保、不具合報告、回収対応、リスク管理、市販後の安全性監視 など、日本国内で発生するすべての薬事責任を担います。
また、MAH とは異なり、認証/承認取得者は外国製造業者(外国特例認証/承認取得者)となりますが、DMAH はその代理として日本国内での実務上の薬事責任を負います。
外国特例承認制度を使用する場合には、この DMAH の選任が不可欠となります。
弊社の提供する
薬事代行サービス
弊社では(選任)製造販売業者として以下のような薬事代行サービスを提供します。
承認、認証申請、届出
外国製造業者登録
PMDA、
認証機関への相談
一般的名称等の
該当性調査
サーベイランス
審査対応
QMS(定期)
調査申請
通関等輸入に係る業務
販売代理店への出荷
市販後安全管理に係る
業務
不具合等による
回収業務等
保険適用の対応
広告の規制チェック
(薬機法)
薬事申請フロー
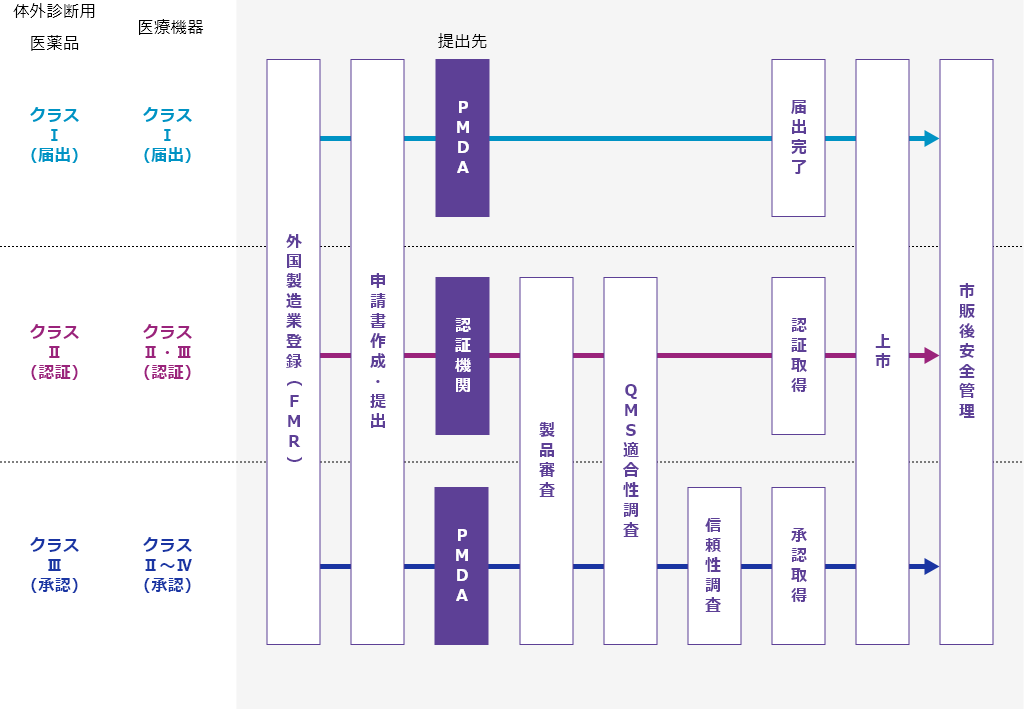
ICSTの特徴
ワンストップサービス
弊社の(選任)製造販売業と製造業を使用することで、製品の申請から検品・包装表示および市場への出荷までの一連の流れを行います。
英語での
コミュニケーション
英語に長けたスタッフが多く、英語によるEメールのやりとり、WEBミーティングを行えます。
広告の規制チェック
(薬機法)
弊社が製造販売する製品の広告は、ご要望があれば法規制に準拠しているか確認させていただいております。
豊富な実績
多岐にわたる医療機器の申請手続きをサポートしてきた実績があります。経験豊富な専門チームが、迅速かつ正確な申請を実現します。

製造販売業者の
役割と申請方式
日本で医療機器を申請するには、医療機器製造販売業の許可が必要です。製造販売業者の関わり方はMAHとDMAHの2つがあります。
-
製造販売業者
(MAH)- 役割:
- ・製造販売業者として、外国製造業者登録の代行および製品申請を行う
- ・QMS省令に基づく品質管理及びGVP省令に基づく製造販売後安全管理業務を実施
- ・市場に対する製造プロセスの実質的責任者及び市場出荷判定の実施者
- ・製品の認可の所有者
- 製造販売承認
- 品質管理
-
-
外国製造業者
(外国特例承認取得者)- 役割:
- ・一社の製造販売業者を選任する
- ・市場に対する製造プロセスの実質的責任者
- ・製品の認可の所有者
- 製造販売承認
- 品質管理

-
選任製造販売業者
(DMAH)- 役割:
- ・外国製造業者に選任された製造販売業者として、外国製造業者登録および製品申請の代行を行う
- ・QMS省令に指定された範囲の管理業務及びGVP省令に基づく製造販売後安全管理業務を実施
- ・外国製造業者の指示で、外国製造医療機器の輸入・製造販売を行う
- ・市場出荷判定の実施者
- 国内品質管理サポート
-
QMS : 品質マネジメントシステム
GVP : 製造販売後安全管理
| MAH申請 | DMAH申請 | ||
| 製造販売業者 | 選任製造販売業者 | 外国製造業者 | |
| 対象の医療機器クラス | Ⅰ~Ⅳ | Ⅱ~Ⅳ | |
| 対象の体外診断用医薬品クラス | Ⅰ~Ⅲ | Ⅱ~Ⅲ | |
| 承認取得者 | 〇 | × | 〇 |
| QMS省令(省令169号) | 〇 | △※ | 〇 |
| GVP省令(省令135号) | 〇 | 〇 | × |
| 製造プロセスにおける責任 | 〇 | × | 〇 |
| 市場出荷判定の実施 | 〇 | 〇 | × |
※QMS省令の第72条の3に規定する業務
〇:責任を負う
△:限定的に責任を負う
×:責任を負わない
MAHの概要図
- ・対象のクラス
医療機器:Ⅰ~Ⅳ
体外診断用医薬品:Ⅰ~Ⅲ - ・製品の認可の保有者:ICST
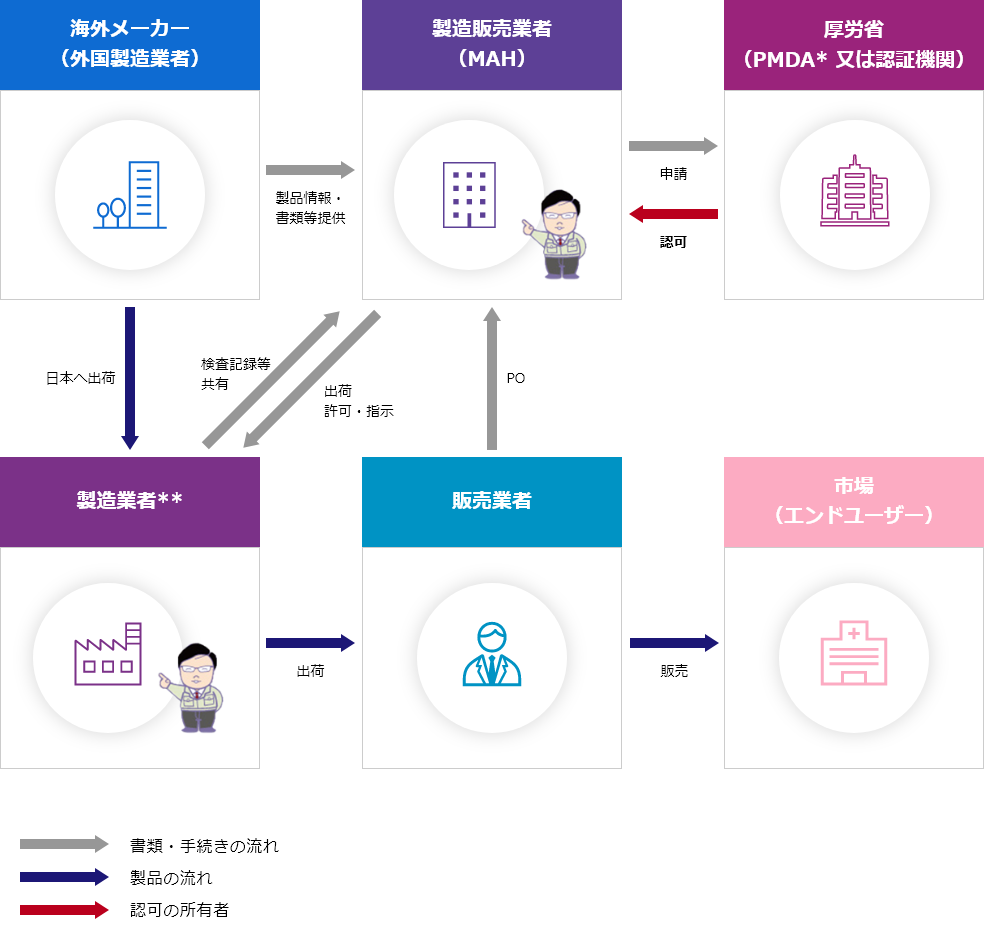
*PMDA:医薬品医療機器総合機構
**ICST製造所、ICSTの委託製造所又は他社の製造所(相談可)
DMAHの概要図
- ・対象のクラス
医療機器:Ⅱ~Ⅳ
体外診断用医薬品:Ⅱ~Ⅲ - ・製品の認可の保有者:海外メーカー
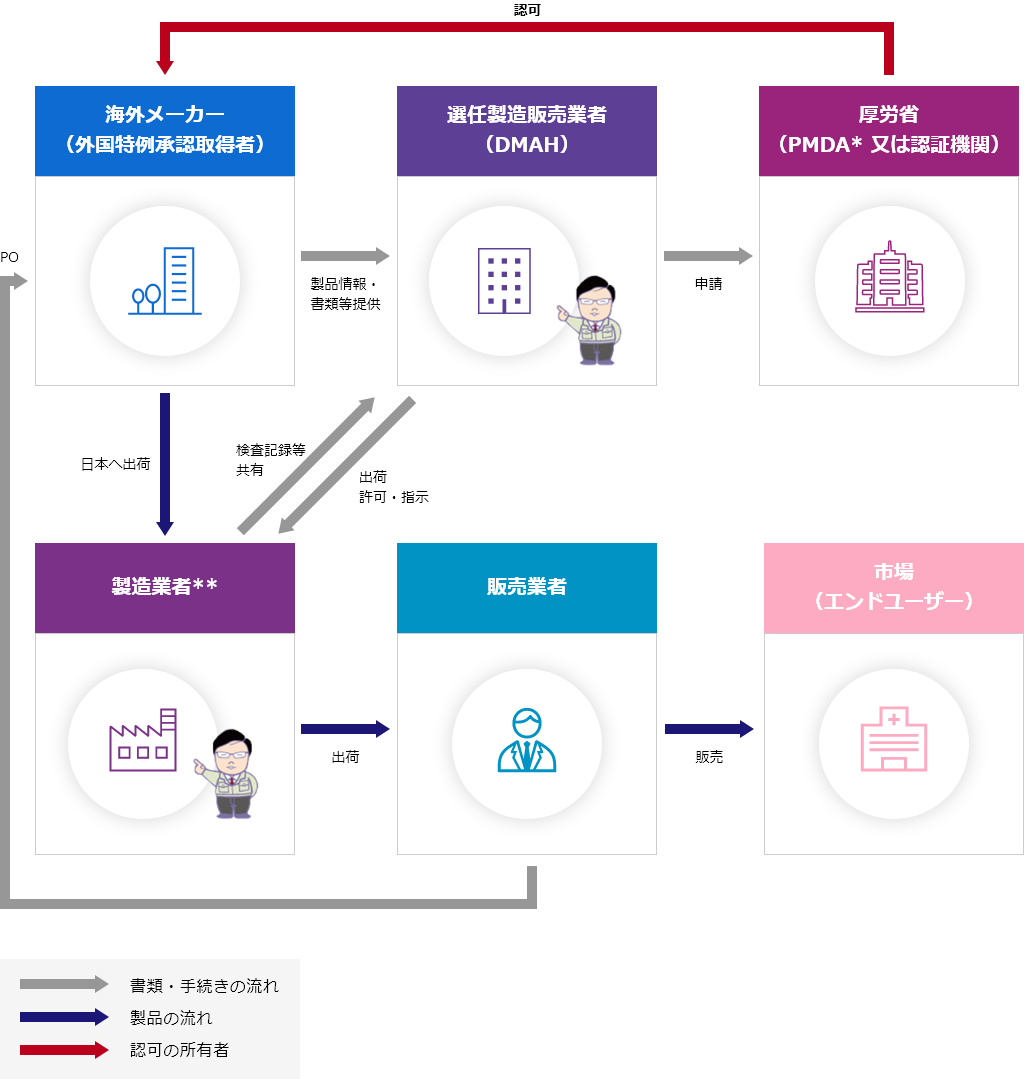
*PMDA:医薬品医療機器総合機構
**ICST製造所、ICSTの委託製造所又は他社の製造所(相談可)
豊富な実績
国名
- ・アメリカ
- ・ドイツ
- ・ベルギー
- ・カナダ
- ・スイス
- ・韓国
- ・スウェーデン
- ・イタリア
- ・中国(深圳・東莞・上海)
- ・デンマーク
- ・オランダ
- ・台湾 など
取扱製品
- ・インスリン皮下投与用針付注射筒
- ・汎用画像診断装置ワークステーション用プログラム
- ・家庭用電位治療器
- ・歯科用多目的超音波治療器
- ・遺伝子解析装置
- ・パルスホルミウム・ヤグレーザ
- ・酸素濃縮装置
- ・パルスオキシメータ
- ・低周波治療器
- ・浸透圧分析装置 など
医療機器/体外診断用医薬品
弊社の最終製品保管製造所のサービス
(ワンストップサービス)
最終製品の保管とは
医療機器/体外診断用医薬品は、市場へ出荷する前に製造販売業者による出荷判定が必要になります。
出荷判定時に製品を保管している施設を「最終製品の保管製造所」と言い、製造業登録をしている必要があります。
弊社では医療機器/体外診断用医薬品の申請だけではなく、認可取得後の製品輸入から保管、包装表示、検品、出荷までサポート致します。必要であればご相談の上、販売・修理のサポートもご対応致します。
製造販売業者(MAH)・選任製造販売業者(DMAH)のいずれでも対応致します。
製造業務委託サービス
- ・受入検査
- ・在庫管理(シリアル番号、使用期限等)
- ・包装表示対応
- ・適した温度による管理(冷蔵保管対応あり)
- ・検品対応
- ・入荷、出荷対応
- ・同梱物の確認
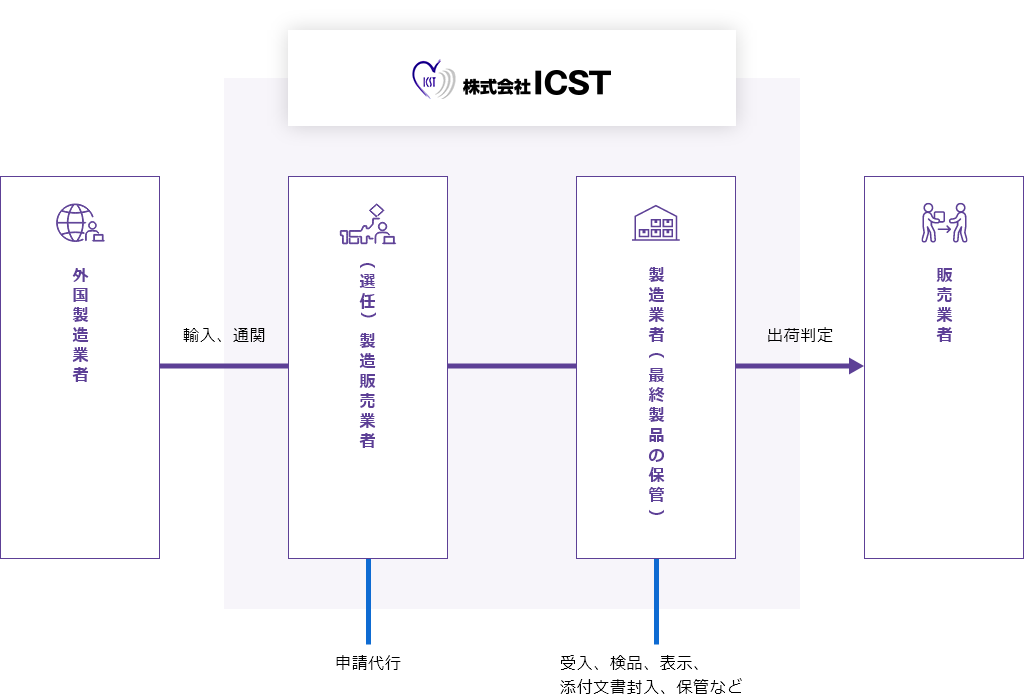
※弊社の保管製造所を使用した場合の例となります。
お客様ご指定の保管製造所でもご対応可能です。
料金システム
(選任)製造販売業
弊社では申請代行費の他、月額固定で「維持管理費」を頂いております。
維持管理費の内容は以下の通りです。
- ・製造販売業務全般
- ー品質管理業務(QMS業務)
- 例:市場への出荷判定、製品関連文書・記録の管理等
- ー安全管理業務(GVP業務)
- 例:安全管理情報の収集・解析等
※1品目ごとの費用(品目が増えれば割引あり)
※仕入数量やインボイス合計金額によって「維持管理費」は変動致しません。
維持管理費は製品の特性とリスク分析による不具合発生率や年間出荷数によりご相談の上で決めております。
製造業
弊社に製造業務(最終製品の保管)を委託される場合、
以下項目に関わる費用を頂いております。
- ・製造業務維持管理費用
- ・製品検査、包装表示費用
- ー受け入れ検査
- ー附属品の同梱確認
- ー添付文書の同梱
- ー法定表示ラベルの発行及び貼付 など
- ・保管費(使用面積及び日数による)
